자연요법 연구소인 허발짐(Herbalzym)에서는 전통적인 방법으로는 치료가 어려운 각종 암(cancer)과 난치성질환의 치료에 과학적 연구결과를 기초하여 개발된 천연물 및 생약 효소제를 사용하는 치료법을 연구.발전시켜왔습니다. 허발짐(Herbalzym) 요법은 지난 10여년간의 임상실험 및 말기환자의 치료를 통해 탁월한 치료효과를 계속 반복하여 입증하고 있습니다.
지난 2010년 12월 부터 16주간의 치료계획으로 순수한 천연의 면역기능조절 성분인 헤파짐(Hepazym)을 복용 중인 만성 B형간염 새 환자분의 6주간 경과입니다. 환자분으로부터 받은 메일입니다.
2010/11/2
저는 만성b형간염환자입니다.
현재 바라쿠르드 0,5mg복용중이구
자연요법으로 죽염,사리장환(서리태,죽염,유황오리,마늘,등으로만든 해독간장)사리장은 인산김일훈선생이만든 것으로 해독작용이 좋다하여 복용중,그리고 청국장,비타민c 6g복용중입니다.현재상태는
got;53 gpt;101이고, e항원항체 정상
바이러스 3350 copie입니다
부모중에 보균자는없으시고 21살때 처음 간염인것을 알고 34살인 지금까지 투쟁중입니다
문제는 비정상적인 간기능수치와 면역반응없이 e항체생성으로 약을 먹지않으면 바이러스증가합니다
자연요법으로 치료하고 싶은데
막막해서 상담합니다
부디 좋은방법 부탁드리며 그리고 공지란에 헤파짐처방이 있든데 그것은무엇인지요? 저에게도 해당되는지요?답변부탁합니다
2010/11/4
안녕하세요 답변고맙습니다
궁금한게있는데 보통 얼마나 먹으면 면역반응이 오나요? 물론 제게도 s항체가 생기면 좋겠지만 근데 바라쿠르드나 비타민c와 함께 복용해도 되나요? 아님 헤파짐만 복용하는것이 좋은지요?
2010/11/5
다른 환자분들은 저처럼 바라쿠르드나 제픽스를 복용하면서 헤파짐을 먹었나요? 궁금한게 너무 많은데 두서없이 적어봅니다,바라쿠르드를 끊고싶은데 악화될까 걱정되어서 쉽게하지 못하네요, 면역반응이 오신 2환자분은 어떻게 치료하였는지도 궁금합니다,아시는 것이 있으면 부탁합니다
그리고 간단히 저의 현재 상태를 적어봅니다…
매년 전세계적으로 진단되는 모든 암의 15-25% 정도는 미생물 감염이 그 원인이거나 또는 발병기전에 작용하는 것으로 많은 과학자들은 믿고 있습니다. 아시아에서 특히 간암발병율이 높은 것은 만성 B형간염 환자가 많기 때문이며, 만성 B형간염은 잠재적 간암유발인자로 간암의 발병과 밀접하게 연관되어 있습니다. 일단 만성 B형간염에 감염되면(대부분 어린시기에 감염) 거의 일생을 함께 합니다.
만성 B형간염 바이러스(HBV) 감염은 전세계적으로 확산되었고, 그 유해성은 심각한 위협이 되고 있습니다. 전세계적으로 약 3억명 이상의 만성 B형간염 환자가 있으며, 특히 만성B형간염 감염율이 높은 지역은 아시아, 아프리카, 태평양군도, 남미와 중동지역입니다. 만성 B형간염 바이러스(HBV)는 체외에서도 약 1주일정도 생존할 수 있으므로 간접적인 접촉으로도 감염될 수 있으나, 주된 전파경로는 신생아기에 부모로부터 물려받는 수직감염이며, 환자와의 성접촉, 혈액이나 체액, 정맥 주사기 등을 통해 전파됩니다.
만성 B형간염 감염은 평생 지속되지 않는 경우라면 대개 수년간 지속됩니다. 만성 B형간염 바이러스(HBV)는 장기간의 증식과정에서 숙주의 면역반응을 피하여 면역체계가 B형간염바이러스를 감지, 증식억제, 제거하는 것을 효과적으로 …
전통적인 암치료법에서는 단지 암세포를 제거하는 것에 대해서 모든 초점을 맞추어 왔으며, 암 줄기세포(cancer stem cells)는 치료목표에서 상대적으로 소외되어 왔습니다. 일부의 암에서는 항암치료를 통해 암세포를 어느 정도 죽이는 효과를 일시적으로 거둘 수는 있겠지만 그러나 소수의 암줄기세포(cancer stem cells)는 항암이나 방사선 치료에도 죽지 않고 살아남아 잠복하며, 후에 다시 암세포 형태로 활발하게 증식하고 신체의 다른 부위로 전이되고 맙니다. 암줄기세포는 단 한 개가 살아남는다고 하더라도, 시간이 경과하면 후에 다시 더욱 공격적인 악성종양 형태로 완전하게 재발하게 됩니다. 그러므로 암 치료법이란 암세포들을 죽이는 목표 외에도 암 줄기세포가 다시 새로운 형태로 증식을 시작하여 더욱 심각한 문제를 일으키기 전에 완전하게 제거되도록 하는 것을 목표로 실행되어야만 합니다. 만일 암 줄기세포를 완전히 사멸시킨다면 암이 완전히 제거(완치)될 것입니다.
세포가 분열하고 노화되는 과정에서 유전자가 관여하는데 그것이 텔로미어(telomere)라는 염색체 끝 부분의 핵산서열로 세포가 분열 할 때마다 조금씩 길이가 줄어들게되며 세포분열의 한계점에서는 텔로미어가 다 없어지고 …
 파테놀리드(parthenolide)는 휘버휴(feverfew) 같은 약용식물의 세스퀴터펜 락톤(sesquiterpene lactones)에서 추출되는 성분입니다. 세스퀴터펜 락톤(sesquiterpene lactones)은 식물에서 유래된 성분으로 여러 식물의 오일에 함유되었으며, 전통적으로 항암, 항염증(항바이러스, 항진균) 효능을 지닌 것으로 알려졌습니다. 임상치료에 사용되는 세스퀴터펜 락톤(sesquiterpene lactones)은 아르테미시닌(artemisinin), 탑시가진(thapsigargin), 파테놀리드(parthenolide) 그리고 여러 합성 유도체(synthetic derivatives)들이 있습니다. 이들 성분들은 암 종양과 암 줄기세포의 특정 신호경로를 표적으로 하는 임상치료에서 선별 적용되고 있습니다.
파테놀리드(parthenolide)는 휘버휴(feverfew) 같은 약용식물의 세스퀴터펜 락톤(sesquiterpene lactones)에서 추출되는 성분입니다. 세스퀴터펜 락톤(sesquiterpene lactones)은 식물에서 유래된 성분으로 여러 식물의 오일에 함유되었으며, 전통적으로 항암, 항염증(항바이러스, 항진균) 효능을 지닌 것으로 알려졌습니다. 임상치료에 사용되는 세스퀴터펜 락톤(sesquiterpene lactones)은 아르테미시닌(artemisinin), 탑시가진(thapsigargin), 파테놀리드(parthenolide) 그리고 여러 합성 유도체(synthetic derivatives)들이 있습니다. 이들 성분들은 암 종양과 암 줄기세포의 특정 신호경로를 표적으로 하는 임상치료에서 선별 적용되고 있습니다.
파테놀리드(parthenolide)는 전통적으로 편두통(migraine)과 류마티스관절염의 치료에 수세기 동안 사용되었으며, 근래에는 실험에서 대장암, 췌장암, 간암, 백혈병, 담도암(cholangiocarcinoma) 같은 다양한 종류의 암세포의 증식 억제와 사멸(apoptosis)을 유도한다는 연구결과가 보고되기도 하였습니다. 또한 파테놀리드(parthenolide)는 내성이 생긴 암세포의 항암제에 대한 감수성을 높일 수 있으며, 동물실험에서는 피부암을 막아주는 작용을 하는 것으로 밝혀졌습니다. 이 외에도 연구보고는 파테놀리드(parthenolide)가 전사인자 NF-kB억제와 STAT-3의 조절, MAP키나제(kinase)의 활성억제, TRAIL이 매개하는 항사멸 단백질의 차단 유도, 미토콘드리아 기능이상, 활성산소종(ROS)의 증가 등의 작용으로 암세포의 …
암이 발생, 진행되고 약물에 대해 내성을 갖게 되는 데에는 종양유전자의 활성화와 종양억제 유전자의 불활성화로 요약할 수 있는 유전자 발현의 후생적 조절(epigenetic control)이 매우 중요한 역할을 합니다. 후생적 조절(epigenetic control)이란 DNA 염기서열이 변하지 않는 상태에서 이루어지는 유전자 발현의 조절을 일컬으며, 몇 가지 화학적변형을 통해 DNA가 팩킹(packing: DNA는 당과 단백질이 단추역할처럼 후크를 만들어 팩킹되어 안전하게 보존되어 있다가 필요시 떼어내 사용) 되는 것을 바꾸는 스위치가 꺼지거나 켜지기 용이하도록 만드는 것입니다. 이러한 패턴의 변화가 자연적으로 활성화되는 것은 무엇보다도 개개인마다 처한 독특한 환경적 요인이나 스트레스, 식습관, 운동, 독성물질에 노출 등에 의해 영향을 받습니다. 유전자발현의 후생적 리모델링(epigenetic remodeling) 동안 나타나는 후생적 변화는 크게 3가지 형태로 구분됩니다.
DNA의 메틸화(methylation): DNA 염기에 메틸기(CH3-)가 붙는 메틸화(methylation)가 종양발생 동안에 이상조절될 수 있으며, 종양억제 유전자를 비롯한 다른 유전자들이 불활성화 됩니다.
히스톤 변형(Histone modifications): 히스톤(histone)은 핵 내에서 DNA와 결합하여 그 작용을 나타내는 주요 단백질로 …
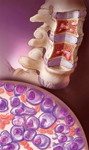 다발성 골수종(multiple myeloma)은 백혈구의 일종인 형질세포(plasma cell)가 무한 생성되어 발생하는 골수(myeloma)의 암입니다. 정상인의 경우는 골수에 형질세포(plasma cell)가 5% 미만의 분포로 면역글로블린(Immunoglobulin: Ig)이라는 항체를 만듭니다. 그러나 다발성골수종(multiple myeloma)에서는 형질세포가 걷잡을 수 없이 증식하여 단일 형태의 면역글로불린(Ig)을 과도하게 생성하므로, 다른 형태의 면역글로불린(Ig) 양이 위험할 정도로 낮게 떨어져서 환자가 감염에 노출됩니다. 암성 형질세포(malignant plasma cell)는 거의 모든 뼈로 전이되어 비정상적인 형질세포로 채워지고 정상적인 뼈가 녹아 내립니다. 그 결과 여러 군데 뼈에 구멍이 나는 증세가 나타나기 때문에 다발성(multiple)이라는 이름이 붙었고, 뼈의 통증과 골다공증, 골절, 그리고 녹아내린 뼈로 인해 혈중 칼슘치가 증가하는 고칼슘혈증(hypercalcemia)이 생기고 콩팥에 손상을 줍니다. 또한 혈액을 만드는 골수를 비정상적인 형질세포가 차지하고 있어 적혈구, 백혈구, 그리고 혈소판이 적게 만들어져 빈혈, 감염, 그리고 출혈 등이 야기됩니다.
다발성 골수종(multiple myeloma)은 백혈구의 일종인 형질세포(plasma cell)가 무한 생성되어 발생하는 골수(myeloma)의 암입니다. 정상인의 경우는 골수에 형질세포(plasma cell)가 5% 미만의 분포로 면역글로블린(Immunoglobulin: Ig)이라는 항체를 만듭니다. 그러나 다발성골수종(multiple myeloma)에서는 형질세포가 걷잡을 수 없이 증식하여 단일 형태의 면역글로불린(Ig)을 과도하게 생성하므로, 다른 형태의 면역글로불린(Ig) 양이 위험할 정도로 낮게 떨어져서 환자가 감염에 노출됩니다. 암성 형질세포(malignant plasma cell)는 거의 모든 뼈로 전이되어 비정상적인 형질세포로 채워지고 정상적인 뼈가 녹아 내립니다. 그 결과 여러 군데 뼈에 구멍이 나는 증세가 나타나기 때문에 다발성(multiple)이라는 이름이 붙었고, 뼈의 통증과 골다공증, 골절, 그리고 녹아내린 뼈로 인해 혈중 칼슘치가 증가하는 고칼슘혈증(hypercalcemia)이 생기고 콩팥에 손상을 줍니다. 또한 혈액을 만드는 골수를 비정상적인 형질세포가 차지하고 있어 적혈구, 백혈구, 그리고 혈소판이 적게 만들어져 빈혈, 감염, 그리고 출혈 등이 야기됩니다.
Multiple myeloma: diagnosis and treatment.
Treatment of …
다음을 생각해 보시기 바랍니다. 가장 큰 문제는 현재 항암치료 약물에 대한 암세포의 내성을 차단할 수단이 전혀 마련되어 있지 않다는 것입니다. 우리는 항암치료 약물 자체를 반대하는 것이 아닙니다. 우리는 거대제약회사의 배를 불리는 것 외에는 거의 아무런 효능이 없는 새로운 독성항암약물을 폭발적으로 사용하는 것에 반대하는 것입니다. 병원에서는 항암제에 내성을 나타내기 이전에 암세포를 죽여야만 하므로, 처음부터 많은 양의 독성약물을 투여하지만, 이로 인해 정상세포마저 파괴되어 신체 기능이 크게 손상되고, …
암 유전자 RAS와 RhoA는 이상적인 동반자로 작용하며, RhoA가 계획된 세포사멸(apoptosis)을 막아내어 암세포가 죽지않고 살아남는 동안, RAS는 암세포의 성장을 강화시킵니다. 양쪽 모두 자연치료제 조르반(Zorvan), 씨놀짐(SinnolZym), 지놀짐(GinolZym), 루테올린(luteolin)을 비롯해 스태틴(statin)계 약물과 좀메타(Zometa)와 액토넬(Actonel)같은 비스포스포네이트(nitrogen bisphosphonates)계 약물을 통해 억제가 가능하다고 앞에서 설명드렸습니다. 아래 연구보고는 비스포스포네이트(nitrogen bisphosphonates) 계 약물의 항암작용에대해 주로 다루었으며, 콜레스테롤 합성경로에서 스태틴(statin)계의 약물과 비스포스포네이트(nitrogen bisphosphonates) 계 약물의 작용에 대해 잘 설명합니다. 다음 연구보고는 스태틴(statin)계 약물이 암 발병을 줄여주는 효능에 대한 좋은 내용입니다. 여기에서는 스태틴(statin)계 약물이 어떤 종류의 암이든 전체적으로 28 %를 줄여주는 결과를 보여줍니다. 이것은 매우 포괄적인 연구지만, 특정 스태틴(statin)계 약물과 차이는 없습니다. 또 다른 연구에서는 스태틴(statin)계 약물을 적정량을 사용하여 혈관을 암세포 속으로 성장하도록 유인하는 VEGF (혈관내피세포성장인자)의 분비 억제를 통해 암세포성장을 억제시키는 것이 매우 중요한 요인임을 보여줍니다. 낮은 용량의 스태틴(statin)계 약물은 혈관신생(angiogenesis)을 촉진하지만 고용량을 사용시에는 GGPP (geranylgeranyl pyrophosphate, 게라닐게라닐파이로인산)의 작용에 의해 반대로 혈관신생을 억제(anti-angiogenesis)합니다. Statins have biphasic effects on angiogenesis. Cerivastatin, an inhibitor of 3-hydroxy-3-methylglutaryl coenzyme a reductase, inhibits endothelial cell proliferation induced by angiogenic factors …
여기에서는 콜레스테롤을 조절하는 자연치료제를 비롯해 스태틴계 약물(statin drugs), 그리고 골다공증 치료약물인 비스포스포네이트(bisphosphon)가 여러 종류의 암치료 효능을 강화시키는 역할에 대해 설명하겠습니다. 암세포를 포함한 인체의 모든 세포조직은 콜레스테롤 없이는 생존이 불가능합니다. 첫째로 인체에 해로운 것으로만 알려진 포화지방(saturated fats)과 콜레스테롤은 인체를 구성하는 모든 세포막(cell membranes)의 약 1/2을 차지하며, 인체부위마다 다른 세포의 종류와 기능에 맞추어 콜레스테롤 필요량이 달라집니다. 인체 세포조직 중에서 특히 뇌세포, 신경세포에는 많은 콜레스테롤을 필요로 하며, 뇌의 도파민 생성, 담즙산, 비타민 D 와 호르몬생성, 면역기능 등에도 필수적입니다. 암세포를 비롯한 인체의 모든 세포가 생존하기 위해서는 반드시 세포막을 통해 세포간 교신(communicate)을 하거나 세포막 내부.외부로 필요한 물질들을 이동시켜야 합니다.암치료의 핵심목표: 콜레스테롤(cholesterol) 대사의 조절 (5)
병원에서 항암치료(chemotherapy)를 받다 보면 대부분 암세포는 얼마 후 내성(drug resistance)을 갖게 됩니다. 이 때 의사들은 항암제 종류를 바꾸어 새로이 시도를 해보지만 바뀐 항암제 역시 효과가 없고 증세가 오히려 더 악화되는 경우가 거의 대부분입니다. 마지막으로 의사들은 새로이 개발중인 신약의 사용을 권하며 임상실험을 하기도 하지만, 역시 효과 없이 한 가닥 희망마저 사라지게 됩니다. 이 단계에 이르면 의사는 집에서 생을 마감하도록 환자를 돌려보냅니다. 물론 이런 일이 절대로 일어나서는 안될 것입니다.암치료의 핵심목표: 콜레스테롤(cholesterol) 대사의 조절 (4)
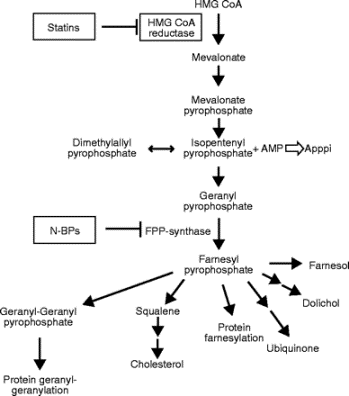 좌측의 도표를 보면 콜레스테롤(Cholesterol) 등을 생합성하는 메발로네이트 경로(mevalonate pathway)에서 스태틴(statins)계 약물은 HMG-CoA 환원효소를, 비스포스포네이트(nitrogen bisphosphonates: N-BPs)는 뼈를 분해하는 역할을 하는 파골세포 기능에 중요한 효소인 FPP (Farnesyl pyrophosphate) 합성효소(synthase)를 강력하게 억제하는 것을 알 수 있습니다. 골다공증 치료제인 비스포스포네이트(bisphosphonates)는 여러 경로에 작용하여 골흡수를 억제하는 작용이 강하므로 특히 유방암, 전립선암, 폐암을 비롯해 뼈로 전이가 …
좌측의 도표를 보면 콜레스테롤(Cholesterol) 등을 생합성하는 메발로네이트 경로(mevalonate pathway)에서 스태틴(statins)계 약물은 HMG-CoA 환원효소를, 비스포스포네이트(nitrogen bisphosphonates: N-BPs)는 뼈를 분해하는 역할을 하는 파골세포 기능에 중요한 효소인 FPP (Farnesyl pyrophosphate) 합성효소(synthase)를 강력하게 억제하는 것을 알 수 있습니다. 골다공증 치료제인 비스포스포네이트(bisphosphonates)는 여러 경로에 작용하여 골흡수를 억제하는 작용이 강하므로 특히 유방암, 전립선암, 폐암을 비롯해 뼈로 전이가 …
암치료의 핵심목표: 콜레스테롤(cholesterol) 대사의 조절 (3)
암치료의 핵심목표: 콜레스테롤(cholesterol) 대사의 조절 (2)
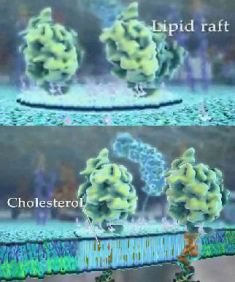 세포막은 다양한 지질분자로 이루어졌습니다. 몇년 전 까지만 해도 세포막은 균일한 유동성을 갖는 이중지질막(lipid bilayer)의 구조를 형성한다고 알려져 있으나 최근에는 당지질(glycolipid)과 콜레스테롤(cholesterol)로 이루어진 지질 라프트(lipid rafts: 지질뗏목)이라고 …
세포막은 다양한 지질분자로 이루어졌습니다. 몇년 전 까지만 해도 세포막은 균일한 유동성을 갖는 이중지질막(lipid bilayer)의 구조를 형성한다고 알려져 있으나 최근에는 당지질(glycolipid)과 콜레스테롤(cholesterol)로 이루어진 지질 라프트(lipid rafts: 지질뗏목)이라고 …
« Older Entries Recent Entries »