자연요법 연구소인 허발짐(Herbalzym)에서는 전통적인 방법으로는 치료가 어려운 각종 암(cancer)과 난치성질환의 치료에 과학적 연구결과를 기초하여 개발된 천연물 및 생약 효소제를 사용하는 치료법을 연구.발전시켜왔습니다. 허발짐(Herbalzym) 요법은 지난 10여년간의 임상실험 및 말기환자의 치료를 통해 탁월한 치료효과를 계속 반복하여 입증하고 있습니다.
녹차의 암예방 작용에서 EGCG가 많은 부분을 담당합니다. 암세포는 복합적인 신호경로들을 생존에 이용합니다. 그러나 EGCG는 매우 강력하므로, 이들 신호경로들을 차단합니다. EGCG는 분명 걍력한 항혈관신생(antiangiogenic) 및 항종양(antitumor) 성분으로, 그리고 항암치료제에 대한 종양세포의 반응 조절제로도 작용합니다.
EGCG는 세포주기를 조절하는 단백질 발현을 변화시키고, 세포사멸에 필수적인 효소 카스파제(caspases)를 활성화시키며, 암유발 전사인자와 전분화능력 유지인자(pluripotency maintain factors)를 억제함으로써 세포자멸사(apoptosis)를 유도하고, 세포증식의 정지(cell growth arrest)를 촉진합니다.
또한 EGCG는 전세포(whole cells)에서 단백질분해효소 복합체인 프로테아솜(proteasome) 억제를 유도합니다. 프로테아솜의 억제는 전사인자 NF-kB의 활성화를 차단하므로, EGCG 같은 프로테아솜 억제제가 암과 림프종 및 백혈병에 강한 치료효과가 있을 것이라는 것이 논리적 결론입니다.
Revisiting the role of EGCG-MAX (Pure Liquid 95% EGCG) in the treatment of all cancers and leukemias
암치료를 위한 EGCG의 피부 사용에 관해 그간 많은 연구들이 수행되었습니다. …
 EGCG (epigallocatechin gallate)는 녹차에 가장 풍부하게 함유된, 그리고 아마도 가장 중요한 카테킨(catechin)일 것입니다. 플라보노이드(flavonoid) 계열에 속하는 카테킨(catechin)은 식물의 대사산물로 항산화작용을 하는 폴리페놀입니다. EGCG는 건강한 세포에서는 산화적손상을 막아주는 강력한 항산화성분으로 작용하지만, 또한 항혈관신생, 항종양 성분으로, 그리고 항암치료제에 대한 종양세포의 반응 조절제로도 작용합니다.
EGCG (epigallocatechin gallate)는 녹차에 가장 풍부하게 함유된, 그리고 아마도 가장 중요한 카테킨(catechin)일 것입니다. 플라보노이드(flavonoid) 계열에 속하는 카테킨(catechin)은 식물의 대사산물로 항산화작용을 하는 폴리페놀입니다. EGCG는 건강한 세포에서는 산화적손상을 막아주는 강력한 항산화성분으로 작용하지만, 또한 항혈관신생, 항종양 성분으로, 그리고 항암치료제에 대한 종양세포의 반응 조절제로도 작용합니다.
수 많은 연구문헌에서 EGCG가 모든 종류의 암세포에 살상능력이 있음을 보여줍니다. EGCG는 암세포에서 후생유전적(epigenetically)으로 침묵하는 유전자발현을 재활성화시키고, 세포주기조절 관련 단백질발현의 변환 및 세포사멸 관련 단백질 카스파제(caspases)의 활성화, 전사인자 NF-kB의 억제를 통해 세포자멸사(apoptosis)를 유도하고, 세포성장억제를 촉진합니다.
인체의 주요 암에서는 p53 신호경로의 불활성화가 자주 나타납니다. p53은 인체 암에서 가장 자주 돌연변이가 발생하는 종양억제유전자의 하나입니다. EGCG는 p53의 생리적활성 조절기전의 부분적 기능으로 보이는 히스톤탈아세틸화효소(HDACs)를 억제함으로써 p53의 아세틸화(acetylation)와 전사작용을 증가시킵니다. 카르복시 말단(carboxy terminal) 부분 라이신잔기(lysine residues)에서 p53의 아세틸화(acetylation)는 세포주기정지 및 세포자멸사(apoptosis)와 관련한 p53의 전사작용을 강화시킵니다.
EGCG가 유도하는 p53단백질 안정화의 결과로 …
거의 모든 신경계질환은 면역기능과 연관되어 있습니다. 면역계는 신경계뿐만 아니라 기본적으로 인체의 어느 질환에든 중요합니다. 많은 질환이 만성염증 또는 면역계가 자신의 신체조직을 공격하는 자가면역 요인으로 인해 발병합니다. 어느 질환이든 이런 비정상적인 면역반응에서 기인한 것이 자가면역질환입니다.
신경계질환의 주된 요소는 분명 “자가면역”입니다. CIDP (만성염증성 탈수초성 다발신경병증), GBS (길리안바레 증후군: 급성 다발성신경염) 및 MMN (다초점 운동 신경병증) 같은 신경병증은 자가면역기전에 의해 발생합니다. 신경의 자가면역은 중주신경계 또는 말초신경계 내 거의 모든 조직을 표적으로 삼을 수 있으며, 매우 특이한 방식으로 아주 특정한 세포들을 자주 표적으로 삼습니다.
CIDP는 말초신경, 즉 뇌와 척수 바깥의 신경조직에 가장 흔히 나타나는 만성염증성질환입니다. 신경세포 축삭(axons) 주위를 둘러쌓는 피막인 마이엘린(myelin)이 자가면역 공격을 받아 파괴되면 탈수초화(demyelination)가 진행됩니다. 탈수초화(demyelination)는 신경을 둘러싼 지방질 백색 피막의 절연체가 파괴되는 것입니다. 마이엘린(myelin)의 손실은 지각신경, 운동신경 또는 자율신경에 나타날 수 있습니다. CIDP는 지각 및 운동장애 증상이 서서히 확산되는 질환입니다.
CIDP는 사지의 근력약화를 비롯해 …
만성 염증성장질환(궤양성대장염과 크론병)의 원인은 밝혀지지 않았습니다. 그러나 젊은이들에 매우 흔한 이 만성질환의 발병에는 장관면역계(bowel immune system)가 감염에 노출되는 것이 역할을 하는 것으로 여기고 있습니다.
어떤 염증성장질환 환자들은 위장관의 증상과 함께 다양한 장외증상(extra-intestinal symptoms)을 겪기도 합니다. 이들 장외증상에는 피부자극(결절성홍반), 안구질환(상공막염), 관절통(관절염)이 포함될 수 있습니다. 또한 어떤 환자들은 구강궤양(구강 아프타성 궤양)이 생기기도 합니다.
염증성질환인 베체트 증후군(Behçet’s syndrome)은 눈, 비뇨기, 피부, 관절, 혈관, 뇌, 위장관 등을 포함한 여러 신체기관에 영향을 미치며, 통증을 동반한 재발성 구강궤양을 일으킬 수 있습니다. 유전적요인과 더불어 미생물감염 같은 환경적 요인 모두 베체트 증후군의 발병에 기여하는 것으로 의심되는 요인입니다. 또한 일반적으로 두 가지의 별개질환으로 여기는 베체트 증후군과 염증성장질환은 위장관 및 전신성 증상의 특징들이 많은 부분 서로 겹칩니다.
A case of intestinal Behcet’s disease similar to Crohn’s colitis.
Potential Infectious Etiology of …
인체에 들어있는 가장 많은 미량원소는 뼈를 구성하는 칼슘과 인(phosphorus)이며, 그 다음이 유황(sulfur)입니다. 유황은 거의 대부분 필요량을 우리의 식이를 통해 섭취할 수 있으며, 유황함유 단백질에 정상적으로 들어있는 20종류의 아미노산 중 현재까지 확인된 단 두 종류의 유황 아미노산만이 유황의 주 공급원입니다. 유황함유 아미노산은 메티오닌(methionine)과 시스테인(cysteine)이며, 주로 붉은색 육류와 유제품(dairy products)에 많이 들어있습니다. 단백질에는3%-6%의 유황아미노산(sulfur amino acids)이 함유되어 있습니다. 우리는 아주 적은양의 유황을 무기유황(inorganic sulfates) 형태로, 그리고 마늘과 양파, 브로콜리 같은 식품에 함유된 다른 형태의 유기유황(organic sulfur)으로부터 얻게됩니다. 유황아미노산 두 가지의 대사작용은 밀접하게 연관되어 있습니다. 메티오닌(methionine)은 포유류의 대사작용에서 많은 핵심역할을 하는 필수아미노산(반드시 식이를 통해 섭취)입니다. 메티오닌(methionine)은 사람의 간에서 시스테인(cysteine)으로 전환되는 전구체(precursor)입니다. 시스테인(cysteine)은 상당한 필요량이 체내에서 메티오닌(methionine)으로 부터 합성되므로 준필수아미노산(semiessential amino acids)으로 분류됩니다. 또한 메티오닌(methionine)은 시스테인(cysteine)으로 부터 재생될 수는 없으므로, 베타인(콜린이 산화되어 베타인으로 전환됨), 엽산(folate), 또는 비타민B12 (Cobalamin) 같은 메틸기(단일 탄소) 공여체를 이용하는 호모시스테인(homocysteine)의 메틸화를 통해 …
전세계적으로 수백만명의 사람들이 가장 고통스러운 양대 소화기질환인 궤양성대장염(Ulcerative Colitis: UC)과 크론병(Crohn’s Disease: CD)으로 심히 고통받고 있습니다. 두 질환은 의학분류에서 염증성장질환(Inflammatory Bowel Disease: IBD)에 속합니다 (베체트병도 염증성장질환으로 분류). 염증성장질환에서 염증매개물질(inflammatory mediators)이 확인되었으며, 이들 매개물질들이 염증성장질환의 임상병리적 특징에서 중요한 역할을 한다는 믿을만한 증거들이 제시되었습니다. 그 결과는 정상적인 신체조직을 파괴하는 면역반응입니다. 그러나 염증성장질환이 자가면역질환(autoimmune disease)이라는 과학적 증거는 없습니다. 이는 단지 추정입니다. 염증성장질환의 발병원인은 아직까지 불분명합니다. 염증성장질환은 북부 유럽과 …
종양세포의 비정상적인 대사작용은 이를 치료의 표적으로 활용하는 기회를 제공합니다. 종양세포는 정상세포조직에 비해 메티오닌(methionine)의 제한에 더욱 민감하며, 이를 메티오닌 의존 영양요구(methionine auxotrophy) 현상이라고 합니다. 메티오닌(methionine)은 포유동물의 대사작용에서 단백질 합성과 DNA의 메틸화, 폴리아민(polyamine) 생합성 같은 여러 핵심적 역할을 하는 필수아미노산의 일종이나, 체내에서 생성되지 못하므로 반드시 식이로 공급되어야만 합니다. 여러 암세포와 주요 종양들은 메티오닌(methionine)이 절대적으로 필요합니다. 종양세포에서 메티오닌(methionine) 의존성의 증가는 특정한 대사결함(metabolic defect)의 하나입니다. 메티오닌(methionine) 의존성에 관한 생화학적 기전이 광범위하게 연구되었으나, 근본적 기전은 아직까지 명확하지 않습니다. 메티오닌 고갈(methionine starvation)은 종양세포의 DNA 메틸화, 세포주기 진행, 폴리아민(polyamine)과 항산화물질의 생합성을 강력하게 조절할 수 있습니다. 그러므로 저 메티오닌(low methionine) 식이는 암의 증식, 특히 유방암, 대장암, 전립선암, 폐암을 비롯해 생존과 증식에 메티오닌 의존성을 보이는 다른 암들을 조절하는 중요한 전략의 하나일 것입니다. 이와는 반대로 정상세포는 외인성의 메티오닌 제한(methionine restriction)에 비교적 잘 견딥니다. A review of methionine dependency and the role of …
비터멜론의 씨와 열매 그리고 전체식물에서 다음과 같은 유래 화합물들이 분리, 보고되었습니다. 제2형 당뇨병 환자분들은 그들의 혈중 포도당을 근육에서 에너지로 변환시키는 능력에 이상이 생긴 것입니다. 이것은 일부는 인슐린을 충분히 생산하지 못하는 …
STAT 계열 전사활성조절단백의 일원인 STAT3 (signal transducer and activator of transcription3)는 본래에는 활성화되지 않은 형태로 세포질(cytoplasm) 내에 존재합니다. STAT 단백질은 때로는 “DNA 결합인자”라고 불리는 그룹의 일부입니다. 이들 단백질은 DNA 염기서열에 결합하며, 그리하여 DNA에 있던 유전정보가 RNA로 옮겨가는 전사(transcription)의 과정을 조절합니다. STAT3는 다양한 성장인자(growth factors)와 사이토카인(cytokines)에 의해 STAT3 전사활성 도메인(transactivation domain) 내의 타이로신 잔기(tyrosine residue)가 인산화 됨으로써 활성화됩니다. 인산화된 STAT3 (p-STAT3)는 핵(nucleus) 안으로 들어오게 되며, 종양형성에 관련된 광범위한 표적유전자의 발현을 유도합니다. 종양세포는 성장을 지속하고, 세포자멸사(apoptosis)를 피하기 위해 STAT3에 의존합니다. STAT3는 대장암, 간암, 유방암, 전립선암, 다발성골수종(multiple myeloma), 교모세포종(glioblastoma)을 포함한 광범위한 종양에서 상시 활성화되어 있습니다. 아마도 사람의 모든 종양의 절반 이상이 활성화된 STAT3를 상시 지니고 있을 것입니다. 상시 활성화된 STAT3, 그리고 어느 정도의 STAT5는 종양세포의 증식과 생존, 침윤을 증가시키고, 한편으로는 항종양면역을 억제합니다. STAT3 …
앞서 설명드린 것처럼, PFK1 (phosphofructokinase type 1)은 당분해과정(glycolysis)을 조절하는 주요한 효소입니다. 당분해 효소(glycolytic enzyme) 억제제의 효과적인 암세포 살상작용 (1) PFK1은 4개의 서브유닛(소단위)로 구성된 알로스테릭 효소(allosteric enzyme)이며, 여러 활성물질과 억제물질에 의해 조절됩니다. PFK1은 당분해과정(glycolysis)에서 중요한 위임된 단계(committed step)를 촉매하여, 프럭토스6인산(fructose 6-phosphate)과 ATP를 프럭토스1,6인산(1,6-bisphosphate)과 ADP로 변환시킵니다. PFK1은 고농도의 ATP에 의해 억제되지만, 그러나 AMP는 ATP의 억제작용을 역전시킵니다. 따라서, 세포의 ATP/AMP 비율이 저하될 때 PFK1 효소의 활성이 높아집니다. 따라서, 당분해과정은 에너지 전하(energy charge)가 떨어질 때 촉진됩니다. PFK1은 ATP에 대한 친화도가 다른 기질(substrate:반응물질)과 억제물질 양쪽의 반응 사이트(sites)를 가지고 있습니다. 글루카곤(glucagon)은 PFK1의 합성억제를 통해 PFK1을 억제합니다. 글루카곤(glucagon) 은 혈당 대사작용 조절에 중요한 역할을 하는 호르몬으로, 혈중 혈당의 농도가 어느 수준 이하로 낮아지면 간에서 인슐린과는 반대로 작용하여 혈당량을 상승시킵니다. 또한 PFK1은 …
궤양성대장염과 크론병: 영양요소와 염증성장질환(IBD) 간의 연계
궤양성대장염과 크론병: 염증성장질환(IBD)의 원인은 무엇인가? 지놀짐+오랄짐 요법 케이스
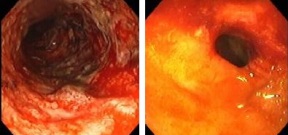 궤양성대장염과 크론병은 여러 장외 증상들(extraintestinal manifestations)이 공통적이나, 일부 장외 증상들은 한 질환에 더 자주 나타나는 경향을 보입니다(빈도의 차이). 궤양성대장염과 크론병은 일상생활을 어렵게하는 증상들(다량의 출혈성 설사, 복부통증, 체중감소 등)의 원인이며, 강력한 항염증/면역억제 약물에 장기간 의존하게 되고, 흔히 장 절제수술로 쇠약해지거나, 심지어 사망하기도 합니다. 궤양성대장염과 크론병은 별개의 질환이라기 보다는 단지 같은 발병원에 두 가지의 다른 증상처럼 보입니다.
궤양성대장염과 크론병은 여러 장외 증상들(extraintestinal manifestations)이 공통적이나, 일부 장외 증상들은 한 질환에 더 자주 나타나는 경향을 보입니다(빈도의 차이). 궤양성대장염과 크론병은 일상생활을 어렵게하는 증상들(다량의 출혈성 설사, 복부통증, 체중감소 등)의 원인이며, 강력한 항염증/면역억제 약물에 장기간 의존하게 되고, 흔히 장 절제수술로 쇠약해지거나, 심지어 사망하기도 합니다. 궤양성대장염과 크론병은 별개의 질환이라기 보다는 단지 같은 발병원에 두 가지의 다른 증상처럼 보입니다.암세포의 메티오닌(methionine) 의존성과 메티오닌(methionine) 식이제한
다양한 종류 암의 치유 효능을 지닌 비엠짐 (비터멜론 추출물 발효 정제)
 비터멜론(bitter melon: Momordica charantia)은 박과(오이, 호박 및 수박) 식물의 일원입니다. 비터가드(bitter gourd) 또는 야생오이(wild cucumber)라고도 불리는 비터멜론 열매는 열대 및 아열대 기후에서 성장합니다. 비터멜론은 높은 치료적 효용가치를 지닌 영양이 풍부한 식물입니다. 비터멜론은 식품으로 그리고 제2형 당뇨와 암, 감염질환, 에이즈(HIV), 월경장애 및 면역질환의 치료를 위한 치료제로도 이용됩니다.
비터멜론(bitter melon: Momordica charantia)은 박과(오이, 호박 및 수박) 식물의 일원입니다. 비터가드(bitter gourd) 또는 야생오이(wild cucumber)라고도 불리는 비터멜론 열매는 열대 및 아열대 기후에서 성장합니다. 비터멜론은 높은 치료적 효용가치를 지닌 영양이 풍부한 식물입니다. 비터멜론은 식품으로 그리고 제2형 당뇨와 암, 감염질환, 에이즈(HIV), 월경장애 및 면역질환의 치료를 위한 치료제로도 이용됩니다.
배당체(Glycosides): 모모딘(momordin), 카란틴(charantin)
알카로이드(Alkaloids): 모모디신(momordicin)
기타: 폴리펩티드(polypeptide)-P
오일(씨에서만): 스테아린산, 리놀산, 올레산
당단백질(Glycoproteins): 알파-모모카린, 베타-모모카린, 렉틴
기타: 비신(vicine: 피리미딘 뉴클레오사이드), MAP30 단백질
커쿠비탄 트리터페노이드(Cucurbitane triterpenoids)
비터멜론 추출물은 혈당과 체지방을 낮춰주는 성분임이 이미 연구를 통해 알려졌습니다. 비신(Vicine), 카란틴(Charantin), 폴리펩티드-P(Polypeptide-P)를 포함한 비터멜론에 들어있는 성분들은 간과 근육, 그리고 지방세포에서 혈당의 흡수와 글리코겐 합성을 증가시키고, 내당능(glucose tolerance)을 개선합니다.당분해 효소(glycolytic enzyme) 억제제의 효과적인 암세포 살상작용 (3)
당분해 효소(glycolytic enzyme) 억제제의 효과적인 암세포 살상작용 (2)
« Older Entries Recent Entries »