아연은 남성호르몬 테스토스테론(production)의 생산에 필요하며, 전립선암의 진단과 진행을 측정하는 표지자인 PSA (전립선특이항원)의 효소적 활성을 억제합니다. PSA는 전립선 세포에서 만들어져 정액으로 분비되는 단백질입니다. PSA는 전립선 특이항원이지 전립선암 특이항원이 아닙니다. 그러므로 PSA 수치의 상승은 전립선암 이외에도 전립선염이나 전립선비대증 같은 일련의 증상에서도 나타납니다.
PSA는 전립선암 세포의 증식과 전이, 침윤에서 역할을 합니다. PSA는 분자량이 약 33 kDa인 세린 프로테아제(serine protease)라는 효소의 일종입니다. 세린 프로테아제는 다른 단백질의 특정 펩티드 결합을 절단(분해)하는 효소군입니다. 포유동물에서 세린 프로테아제는 많은 중요한 기능을, 특히 소화와 혈액응고 및 보체계(complement system: 혈장에 있는 약 30여종의 단백질로 구성된 다기능 방어시스템)에서 기능을 수행합니다. PSA의 세린 프로테아제 작용은 전립선암의 침윤과 전이에 관련되어 있습니다.
PSA는 실제로 시메노젤린(semenogelin 1, 2)이라는 정액단백질(semen proteins)을 분해시키는 효소며, 그 결과로 액화(liquefaction)가 일어나고 정자에 활발한 운동성을 부여합니다. 전립선은 신경을 포함한 주위 연부조직이 결합된 결합조직(connective tissue) 피막으로 싸여 있습니다. 만일 남성호르몬에 의해 조절되는 PSA 의 합성이 과도해지면, PSA는 전립선 내에서 결합조직을 분해시킬 수 있습니다. 암의 전이에는 신체의 한 기관에서 다른 신체부위로 암세포를 확산시키고 침윤토록 하는데 필요한 결합조직의 분해가 수반되어야만 합니다.
이것은 만일 전립선암 세포가 체내에 이미 존재하고 있다면, PSA가 암세포의 증식과 침윤 또는 암세포의 전이성 기능에 절대적으로 기여할 수 있다는 뜻입니다. PSA는 세포외 기질(extracellular matrix)의 세포부착성 당단백질인 피브로넥틴(fibronectin)과 라미닌(laminin)을 분해하며, 그리하여 전립선암세포의 침윤을 용이하게 만드는 것으로 보입니다. PSA의 세포외 기질 분해능력때문에 PSA가 전립선암 조기발견을 위한 표지자일 뿐만 아니라 전립선암의 예방과 진행억제를 위한 표적으로 대두됩니다. 아연이온은 PSA의 활성을 강력하게 억제합니다. 전립선의 아연이온은 PSA의 단백질분해작용 조절을 통해 전립선암 세포의 침윤과 전이를 억제합니다. 간단히 말해서, 아연은 고도의 전이성 전립선암 세포의 증식을 억제합니다.
Presence and enzymatic activity of prostate-specific antigen in archival prostate cancer samples.
Semenogelins I and II bind zinc and regulate the activity of prostate-specific antigen.
Prostate-specific antigen, a serine protease, facilitates human prostate cancer cell invasion.
텔로미어(telomeres)는 염색체(chromosomes)의 양 끝에 붙어 있는 구아닌(guanine)이 풍부한 반복염기서열(repeated sequences)입니다. 그러나 텔로미어는 세포분열(DNA복제)이 될 때마다 조금씩 줄어들게 됩니다. 세포분열시마다 텔로미어가 줄어드는 것은 세포증식 능력을 제한하는 일종의 생체시계 기능입니다. 어느 시점에 이르러 텔로미어의 길이가 매우 짧아지고 임계길이(critical length)에 도달하면 염색체는 더 이상 분열을 할수 없게 됩니다. 이것은 세포가 노화되고, 세포자멸사 과정(apoptotic process)에 의해 죽는 다는 뜻입니다.
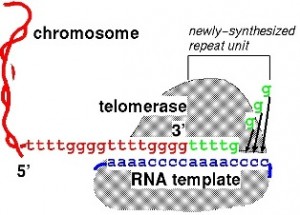 텔로머라제(telomerase)는 염색체 끝부분 텔로미어를 연장하여 세포가 파괴되지 않도록 보호하는 효소(말단소립 복제효소)입니다. 만일 세포에서 텔로머라제가 활성화되면, 세포는 계속 증식과 분열을 할 것입니다. 암세포는 길이가 매우 짧은 텔로미어를 가지고 있습니다. 이들 암세포가 죽지 않고 살아남도록 지켜주는 단 한가지는 효소 텔로머라제의 과발현입니다. 모든 암세포의 85% 이상에서 텔로머라제가 발현되므로, 텔로머라제를 거의 보편적 암세포 표지물질로 여기지만, 대부분의 정상적인 체세포(somatic cells)에서는 텔로머라제가 발현되지 않습니다. 쥐의 실험에서는 텔로머라제 활성화를 재개하면 손상된 세포조직이 수리되고 노화진행을 되돌리는 것으로 나타났습니다.
텔로머라제(telomerase)는 염색체 끝부분 텔로미어를 연장하여 세포가 파괴되지 않도록 보호하는 효소(말단소립 복제효소)입니다. 만일 세포에서 텔로머라제가 활성화되면, 세포는 계속 증식과 분열을 할 것입니다. 암세포는 길이가 매우 짧은 텔로미어를 가지고 있습니다. 이들 암세포가 죽지 않고 살아남도록 지켜주는 단 한가지는 효소 텔로머라제의 과발현입니다. 모든 암세포의 85% 이상에서 텔로머라제가 발현되므로, 텔로머라제를 거의 보편적 암세포 표지물질로 여기지만, 대부분의 정상적인 체세포(somatic cells)에서는 텔로머라제가 발현되지 않습니다. 쥐의 실험에서는 텔로머라제 활성화를 재개하면 손상된 세포조직이 수리되고 노화진행을 되돌리는 것으로 나타났습니다.
대부분의 진행된 암에서는 텔로머라제가 재활성화되어 텔로미어의 길이를 유지시키며, 또한 새로운 연구보고에서는 텔로머라제가 직접적인 암 촉진경로 조절능력을 지닌것으로 드러났습니다. 그러나 암세포에서 텔로머라제가 활성화되는 데 관한 작용기전은 아직 확실하게 밝혀지지 않았습니다. 따라서, 텔로머라제 활성을 억제하는 것은 모든 암치료에 유용한 보편적 표적입니다. 불행하게도 아연은 텔로머라제의 활성을 강화시킵니다.
인돌3카비놀(Indole-3-carbinol: I3C)은 십자화과 식물(양배추, 브로콜리, 컬리플라워, 브루셀 스프라우트)에서 추출된 항암성분의 파이토케미칼 입니다. I3C는 체내에서 에스트로겐 (estrogen) 수치를 낮추는 일련의 반응을 일으킵니다. I3C는 간에서 에스트로겐의 대사를 촉진하고, 유해한 에스트로겐(16-hydroxy estrogen)에 대한 유익한 에스트로겐(2-hydroxy estrogen)의 비율을 높여줍니다. 유익한 에스트로겐(2-hydroxy estrogen)은 유해한 에스트로겐(16-hydroxy estrogen)보다 덜 활성화되며, 일반적으로 체내에서 더 빠르게 소진됩니다. I3C는 남녀 모두에서 건강한 호르몬균형을 유지토록 도와주며, 따라서 유방, 전립선 및 다른 생식기관이 건강하도록 보조합니다.
I3C는 위에서 위산에 의해 DIM(diindolylmethane)으로 변환됩니다. 섭취한 대부분의 I3C는 소장에서 DIM으로 흡수되므로, 십자화과 식물과 I3C의 유익 활성성분이 DIM인 것으로 여깁니다. DIM은 선택적으로 에스트로겐 수용체에 결합하는 것으로 밝혀졌으며, 생리적 농도(physiological concentration)에서 에스트로겐에 길항(estrogen antagonist)하는 작용을 하는 것으로 보입니다. I3C와 DIM은 둘 다 잠재적 발암인자들(carcinogens)을 대사시키는 생화학적 신호경로를 유도합니다. 연구보고는 DIM이 남성호르몬 의존형 전립선암 세포에서 변성남성호르몬인 DHT(dihydyrotestosterone)가 그 수용체에 결합하는 것을 억제하고, DNA합성 유도를 감소시킨다는 것을 보여줍니다.
I3C는 처음에는 잠재적인 유방암 예방작용과 자궁경부암의 원인인 파필로마 바이러스(human papilloma virus: 인유두종 바이러스) 감염환자에게 유익한 작용에 관해 연구되기 시작했습니다. 그러나, 지속된 새로운 연구를 통해 십자화과 식물에서 유래된 I3C가 유방암, 전립선암, 자궁내막암, 대장암, 백혈병을 포함한 여러 암을 억제시킬 수 있다는 것이 밝혀졌습니다. I3C는 텔로머라제 효소의 합성과 활성을 모두 억제합니다. 또한 I3C는 전립선암 세포에서 PSA (전립선특이항원)의 생산을 억제합니다. 최근 연구보고는 I3C가 DNA 복제를 차단함으로써 암세포의 분열을 막아주고, 증식을 억제한다는 결과를 지속적으로 확인해줍니다. 더욱이 I3C는 암세포에서 세포자멸사(apoptosis)를 촉발시킵니다.
I3C는 보충제이므로 처방없이 구입할 수 있습니다. 전립선암 치료를 위해 사용된 복용량은 하루 800 mg 까지입니다. 남성의 일반적인 일일 복용량은 식후 400 mg 복용입니다. 프로스타짐 (ProstaZym)에는 I3C / DIM 복합성분이 들어있으며, 이들 복합성분의 완전한 흡수와 생체이용을 높이기 위해 특별한 효소적 처리과정을 거쳤습니다. 프로스타짐 (ProstaZym)의 생체이용율은 DIM이나 불안정한 전구체인 I3C와는 비교할 수 없이 우월하므로, 프로스타짐 (ProstaZym) 사용으로 적정용량과 시종일관된 효능을 확신할 수 있을 것입니다.
또한 프로스타짐 (ProstaZym)은 여러 십자화과 채소의 활성성분인 PEITC (phenethyl isothiocyanate)를 함유하고 있습니다. PEITC가 지닌 항암효능 배후의 작용기전은 아직 완전히 알려지지 않았습니다. 연구보고에서는 PEITC가 안드로겐 수용체 발현의 하향조절이나, 생체내 불필요한 세포증식을 억제하는 CKI(cyclin-dependent kinase inhibitors) p21과 p27의 유도와 같은 유전자의 조절을 매개한다는 것을 제시합니다. 또한 PEITC는 거의 대부분의 전립선암 세포에서 꺼져있는 글루타치온 S-변환효소(glutathione S-transferase) 계열의 해독효소 유전자를 재활성화시키고, 효소의 기능을 회복시킬 수 있습니다. 식용 PEITC는 또 다른 중요한 생체세포 사멸기전인 오토파지(autophagy: 자식작용: self eating) 유도를 통해 전립선암의 진행을 억제합니다.
Is telomerase a viable target in cancer?
The effects of telomerase inhibition on prostate tumor-initiating cells.
Modulation of telomerase activity by zinc in human prostatic and renal cancer cells.
Indole-3-carbinol inhibits telomerase activity and gene expression in prostate cancer cell lines
Plant-derived 3,3′-Diindolylmethane is a strong androgen antagonist in human prostate cancer cells.