여기에서는 콜레스테롤을 조절하는 자연치료제를 비롯해 스태틴계 약물(statin drugs), 그리고 골다공증 치료약물인 비스포스포네이트(bisphosphon)가 여러 종류의 암치료 효능을 강화시키는 역할에 대해 설명하겠습니다.
암세포를 포함한 인체의 모든 세포조직은 콜레스테롤 없이는 생존이 불가능합니다. 첫째로 인체에 해로운 것으로만 알려진 포화지방(saturated fats)과 콜레스테롤은 인체를 구성하는 모든 세포막(cell membranes)의 약 1/2을 차지하며, 인체부위마다 다른 세포의 종류와 기능에 맞추어 콜레스테롤 필요량이 달라집니다. 인체 세포조직 중에서 특히 뇌세포, 신경세포에는 많은 콜레스테롤을 필요로 하며, 뇌의 도파민 생성, 담즙산, 비타민 D 와 호르몬생성, 면역기능 등에도 필수적입니다. 암세포를 비롯한 인체의 모든 세포가 생존하기 위해서는 반드시 세포막을 통해 세포간 교신(communicate)을 하거나 세포막 내부.외부로 필요한 물질들을 이동시켜야 합니다.
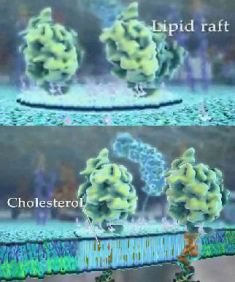 세포막은 다양한 지질분자로 이루어졌습니다. 몇년 전 까지만 해도 세포막은 균일한 유동성을 갖는 이중지질막(lipid bilayer)의 구조를 형성한다고 알려져 있으나 최근에는 당지질(glycolipid)과 콜레스테롤(cholesterol)로 이루어진 지질 라프트(lipid rafts: 지질뗏목)이라고 하는 독특한 지질이 바깥쪽 막에 존재하면서 다른 지질분자와 섞이지 못하고 막의 성분들을 분리시키고 자기들끼리 뭉쳐 매우 역동적으로 막을 구획하는 기능을 담당하는 것으로 밝혀졌습니다. 지질 라프트(lipid rafts: 지질뗏목)는 세포막 수용체와 신호전달 단백질들을 싣고 다닙니다. 수용체는 바이러스가 세포 안으로 침입하는 통로가 되고, 신호전달 단백질은 세포의 성장이나 이동 등 각종 기능 조절에 중요한 역할을 하며, 암세포에서도 AKT를 포함하는 생존경로의 활성화, 증식, 침윤 및 전이에 핵심적인 역할을 합니다.
세포막은 다양한 지질분자로 이루어졌습니다. 몇년 전 까지만 해도 세포막은 균일한 유동성을 갖는 이중지질막(lipid bilayer)의 구조를 형성한다고 알려져 있으나 최근에는 당지질(glycolipid)과 콜레스테롤(cholesterol)로 이루어진 지질 라프트(lipid rafts: 지질뗏목)이라고 하는 독특한 지질이 바깥쪽 막에 존재하면서 다른 지질분자와 섞이지 못하고 막의 성분들을 분리시키고 자기들끼리 뭉쳐 매우 역동적으로 막을 구획하는 기능을 담당하는 것으로 밝혀졌습니다. 지질 라프트(lipid rafts: 지질뗏목)는 세포막 수용체와 신호전달 단백질들을 싣고 다닙니다. 수용체는 바이러스가 세포 안으로 침입하는 통로가 되고, 신호전달 단백질은 세포의 성장이나 이동 등 각종 기능 조절에 중요한 역할을 하며, 암세포에서도 AKT를 포함하는 생존경로의 활성화, 증식, 침윤 및 전이에 핵심적인 역할을 합니다.
암세포는 정상세포보다 증식이 빠르므로 더 많은 콜레스테롤 대사(cholesterol metabolism)를 필요로 합니다. 만일 우리가 자연치료제를 사용해 암세포 특유의 지질대사를 억제하고 적절한 양의 콜레스테롤이 공급되지 못하도록 조절한다면 암세포의 세포막에서 지질 라프트(lipid rafts)가 줄거나 파괴되어 암세포가 죽게되며, 암세포 세포막에 지질라프트(lipid rafts)가 많을수록 이런 현상이 더 잘 일어나 증식이 불가능해지고 또한 세포막 구조에 이상이 생겨 불안정해진 암세포는 스스로 사멸하게 됩니다. 물론 이 경우 암세포는 콜레스테롤 대사가 억제되면 운반을 증가시키는 방법으로 살아남으려 할 것이지만 우리는 세포막에서 콜레스테롤 운반 단백질을 억제하는 자연치료제를 동시에 사용하여 시너지 효과를 얻을 수 있습니다. 그러나 정상세포는 암세포에 비해 안정된 조직이므로 자연치료제에 의한 지질대사 조절에 따른 영향에 안전하며 암세포처럼 죽지 않고 정상적으로 유지됩니다. 우리는 이미 병원치료에서 실패한 말기 암환자의 치료과정에서 이러한 콜레스테롤 대사, 지질대사를 조절하는 방법을 통해 극적인 효과를 경험하고 있습니다.
An update on sphingosine-1-phosphate and other sphingolipid mediators.
The metabolism and function of sphingolipids and glycosphingolipids.
Lipid rafts as a membrane-organizing principle.
Lipid rafts as functional heterogeneity in cell membranes.
Lipid raft-targeted therapy in multiple myeloma.
Membrane remodeling, an early event in benzo[a]pyrene-induced apoptosis.
Ceramide modulates HERG potassium channel gating by translocation into lipid rafts.
The nutritional and clinical significance of lipid rafts.
다음 연구는 암세포막에서 콜레스테롤이 밀집된 부위의 지질 라프트(lipid rafts)가 세포막의 콜레스테롤감소에 의해 어떻게 파괴될 수 있는가를 보여줍니다. 이것은 실로 중요한 연구입니다. 왜냐하면 사람의 심각한 전립선암세포를 특정계통의 쥐에게 이식한 실험을 통해 얻은 결과이기 때문입니다.
콜레스테롤합성을 억제하기 위해 조코(Zocor)를 사용한 이 연구에서 암세포막의 콜레스테롤 감소가 효소AKT와, aka 단백질 키나제(kinase) B의 활성을 억제시켰습니다. 기회가 날 때마다 언급하지만 AKT는 암세포가 살아남도록 하는데 핵심적인 마스터스위치(master switch) 역할을 합니다. 더하여서 암세포가 정상적인 세포자살(apoptosis)을 하지 못하도록 막아내며, 항암치료약물에도 내성을 갖게 만듭니다.
이것은 매우 흥분되는 내용입니다. 이것은 식이요법에서 콜레스테롤의 제한이 콜레스테롤 저하약물복용을 겸하면 함께 상승작용을 일으켜, 말하자면 극도로 불안정한 어느 암종양도 스스로 죽게 만들도록 유도할 수 있다는 것입니다. 연구에서는 전립선암세포를 이식 받은 특수 쥐 중에서 일부는 높은 콜레스테롤식품을 섭취시켰습니다. 단지 6주 후 암종양의 크기의 차이는 놀라운 것이었습니다. 콜레스테롤을 섭취시킨 쥐들은 섭취시키지 않은 쥐들보다 암종양이 2~3배가 커졌습니다. 확실히 콜레스테롤섭취는 암세포증식을 촉진합니다.
통계적으로도 항콜레스테롤 작용을 하는 스태틴(statin)계 약물을 복용하는 사람들은 암발병율이 낮습니다. 그러나, 앞에서 설명한대로 식품의 콜레스테롤을 섭취하면 이러한 약물의 효능을 없애버립니다. 스태틴계 약물은 식이요법에서 콜레스테롤식품을 배제하며 복용해야 합니다. 또한 복용량에 질문이 있을 것입니다. 암세포를 죽이는 목적에는 콜레스테롤을 저하시키는 목적의 복용량보다 20% 혹은 조금 더 사용량을 높여야 합니다. 스태틴(statin)계 약물이 다양한 암종류를 죽이는 데 효과적인 이유는 유전자 RhoA를 세포막에 결합하기 위해 필요한 RhoA의 지질(lipid)변화를 차단시키는 콜레스테롤의 합성을 억제할 뿐만 아니라 RhoA의 억제를 직접 유도함으로써 이러한 항암작용을 합니다.
Inhibition of RhoA or Rac1? Mechanism of cholesterol-independent beneficial effects of statins.
Statin-mediated inhibition of Rho: only to get more NO?
Blockade of the RhoA-JNK-c-Jun-MMP2 cascade by atorvastatin reduces osteosarcoma cell invasion.
Simvastatin and lovastatin inhibit breast cell invasion induced by H-Ras.
만일 RhoA 와 또는 사촌간인 RAS가 지질(lipid)변화를 하지 못한 상태라면, 이들은 암세포막 내피에 결합하지 못하고 비활성상태로 남게 됩니다. 스태틴계 약물의 항암성분에 대해서는 동물실험을 포함하여 수 백 건의 과학적 연구보고가 있습니다. 물론 일반인들은 이러한 연구에 대해 전혀 모릅니다. 이러한 값싼 콜레스테롤 저하 약물이 다양한 종류의 암치료, 특히 뇌종양을 치료에 이용될 수 있다고 알려지면 병원이나 제약회사는 돈벌이가 되지 않기 때문입니다. 스태틴(statin)계 약물은 뇌에 전달될 수 있지만, 대부분의 다른 항암약물은 뇌에 전달될 수 없습니다. 스태틴계 약물은 저렴하고 손쉽게 구입할 수 있는 종류의 치료제입니다.
지금까지 암세포유전자 RAS에 관해서는 별로 언급할 기회가 없었지만, 앞으로는 자주 다루게 될 것입니다. RAS는 가장 유력한 암 또는 종양 유전자일 것입니다. 이것은 모든 암의 적어도 50% 이상에서 활성형태로 변화됩니다. 또한 RhoA는 암에서 거의 변화하지는 않지만 간혹 과도하게 나타나기도 합니다.
계속합니다.
ⓒ 저작권(copyright) 법에 의해 본 사이트(http://www.herbalzym.com)에 게시된 글은 보호받으므로 무단전재 및 재배포를 금지합니다. | 저작권문의는 herbalzym@hotmail.com 으로 하시기 바랍니다.